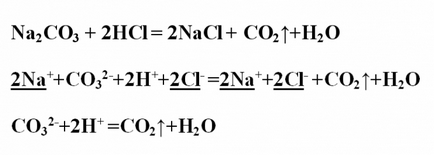Как да пишем йонни уравнения
Преди да започнете да пишете йонни уравнения, трябва да научите някои правила. Неразтворим във вода и malodissotsiiruyuschie газообразно вещество (например, вода) в йони не се разлагат и следователно, да ги записва в молекулна форма. Също така тук са слаби електролити, като H2S, Н2СО3, H2SO3, NH4OH. Разтворимостта на съединения могат да бъдат намерени на разтворимостта на масата, което е позволено референтен материал на всички видове контрол. Там са дадени всички обвинения, които са присъщи на катиони и аниони. За цялостното изпълнение на работата, когато пишете на молекулярно, йон и пълна йон съкращение уравнение.
Пример № 1. запис неутрализация реакция между сярна киселина и калиев хидроксид, го разглежда от гледна точка на TED (теория на електролитна дисоциация). Моля отбележете, реакционната уравнението в молекулна форма и да осигури koeffitsienty.H2SO4 + 2KOH = K2SO4 + 2H2OProanaliziruyte получено вещество на тяхната разтворимост и дисоциация. Всички съединения са разтворими във вода и следователно се разпадат в йони. Единственото изключение е вода, която не се разпада на йони, следователно, да остане в молекулярна йонна vide.Napishite пълна уравнение, да намерите същите йони в лявата и дясната страна, и да се подчертае. За да се намали същите йони, пресича ih.2H + + SO4 2- + 2К + + 2OH- = 2K + + SO4 2- + 2H2OV резултат ще йонните съкращение уравнение: 2Н + + 2OH- = 2H2OKoeffitsienty под формата на двойки може да се намали: Н + + ОН- = H2O
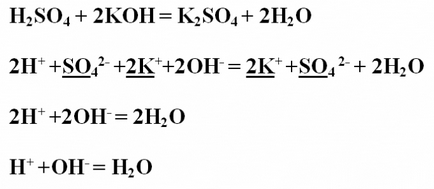
Пример № 2. Реакционната запис обмен между меден хлорид и натриев хидроксид, го разглежда от гледна точка на TED. Запишете реакционната уравнението в молекулна форма и да осигури на коефициентите. В резултат на това, полученият меден хидроксид утаява синьо. CuCl2 + 2NaOH = Cu (OH) 2 ↓ + 2NaClProanaliziruyte всички вещества на тяхната разтворимост във вода - разтворим всичко освен меден хидроксид, който дисоциира в йони няма. Запишете йонен пълна уравнение, стрес и намаляване на същите йони: Cu2 + + 2Cl- + 2Na + + 2OH- = Cu (OH) 2 ↓ + 2Na + + 2Cl-йонни остава съкращение уравнение: Cu2 + + 2OH- = Cu (OH) 2 ↓
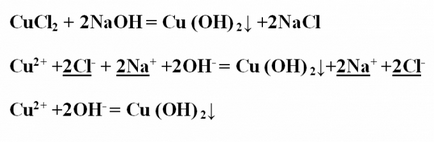
Пример № 3. Добави реакцията обмен между натриев карбонат и хлороводородна киселина, го разглежда от гледна точка на TED. Запишете реакционната уравнението в молекулна форма и да осигури на коефициентите. Получената реакция произвежда натриев хлорид и освобождава газообразен СО2 (въглероден диоксид или въглероден оксид (IV)). Тя се формира от разграждане на слабо въглена киселина разлагане оксид и вода. Na2CO3 + 2HCl = 2NaCl + CO2 ↑ + H2OProanaliziruyte всички вещества в водоразтворимост и дисоциация. Въглероден диоксид напуска системата като газообразно съединение, вода - е malodissotsiiruyuschee вещество. Всички други вещества се разлагат в йони. Запишете йонен пълна уравнение, стрес и намаляване на същите йони: 2Na + + SO3 2- + 2Н + + 2Cl- = 2Na + + 2Cl- + CO2 ↑ + H2OOstaetsya йонен съкращение уравнение: SO3 2- + 2Н + = CO2 ↑ + H2O